El misterio que desconcertaba a los biofísicos durante décadas
Durante años, los investigadores se enfrentaban a una contradicción irritante: inyectar colesterol en una membrana celular la volvía más rígida en algunos experimentos y no la alteraba en absoluto en otros. El resultado parecía caprichoso, impredecible, casi aleatorio. Eso dificultaba construir modelos confiables para aplicaciones tan prometedoras como el drug delivery de precisión, el diseño de células artificiales o el desarrollo de nanoestructuras para biotecnología.
Un nuevo estudio publicado en Nature Communications, liderado por Rana Ashkar de Virginia Tech con colaboraciones de la Universidad de Arizona y la Universidad de Estocolmo, pone fin a esa confusión con una respuesta elegante y con implicaciones prácticas enormes para founders que operan en la intersección entre biología y tecnología.
El hallazgo clave: no importa el qué, sino el cómo se empaquetan
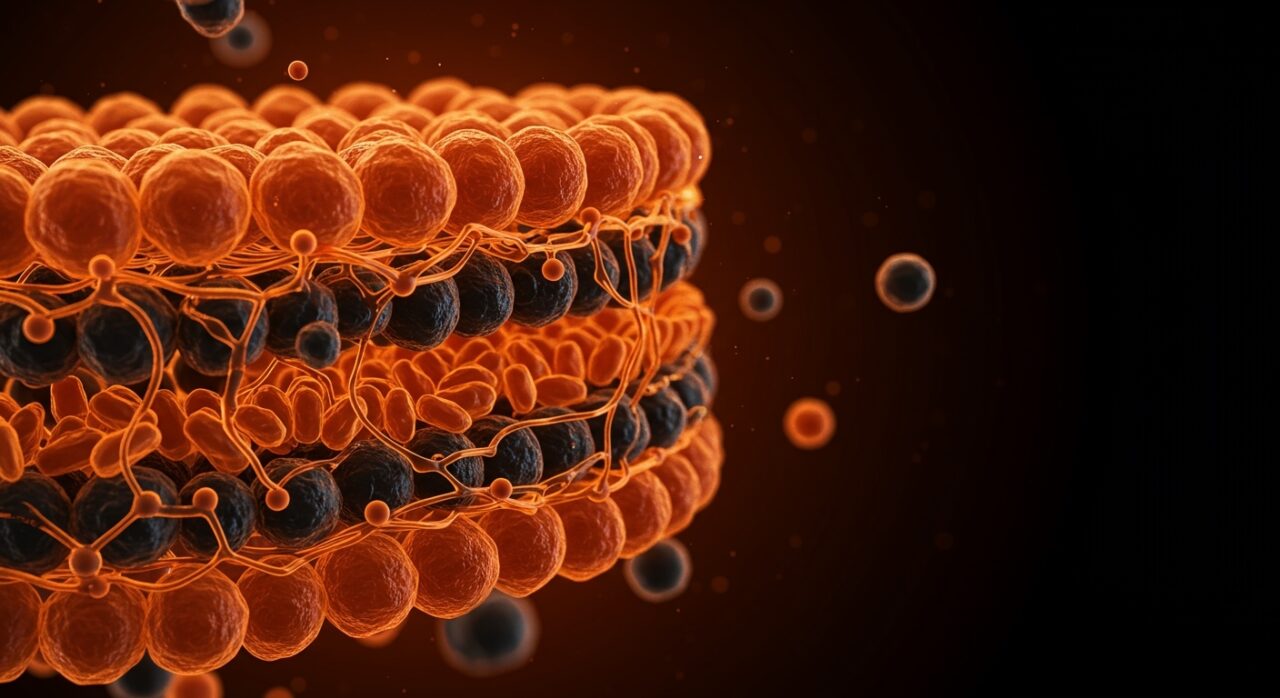
La gran revelación del estudio es que la elasticidad de la membrana celular no depende del tipo de lípido ni de la cantidad de colesterol presente, sino de un único parámetro físico: la densidad de empaquetamiento lipídico, es decir, el área que ocupa cada lípido dentro de la bicapa.
Cuando los lípidos se compactan más, la membrana se vuelve más rígida. Cuando se dispersan, se vuelve más flexible. Así de directo. El colesterol actúa como un modulador de ese empaquetamiento: cambia la forma de los lípidos y ajusta el espacio que ocupan, pero no es el factor determinante en sí mismo. Es el intermediario, no el protagonista.
Este principio fue validado mediante una combinación de técnicas de alta precisión: experimentos con neutrones, difracción de rayos X y simulaciones computacionales, lo que le otorga una robustez experimental difícil de cuestionar.
Por qué esto es una ley física universal y no solo un dato más
Lo que hace especialmente relevante este hallazgo es su carácter de ley física universal a escala mesoscópica. No se trata de un resultado válido únicamente para un tipo de membrana o en condiciones de laboratorio muy específicas. Se trata de un principio general que aplica a una amplia variedad de composiciones lipídicas.
Esto significa que investigadores e ingenieros ahora pueden predecir con exactitud la rigidez o flexibilidad de una membrana simplemente conociendo cómo están empaquetados sus lípidos, sin necesidad de caracterizar experimentalmente cada variante posible. Para quienes trabajan en biotecnología y nanotecnología, eso se traduce directamente en menos iteraciones, menos costos y ciclos de desarrollo más cortos.
Aplicaciones concretas para founders en biotech y deeptech
Este descubrimiento no es solo académico. Sus implicaciones prácticas abarcan varios frentes de alta relevancia para startups y equipos de I+D:
1. Drug delivery y liberación de fármacos
El diseño de vesículas para liberación controlada de fármacos depende en gran medida de controlar la deformabilidad de la membrana. Vesículas demasiado rígidas no se fusionan bien con las células objetivo; demasiado flexibles, se rompen antes de llegar. Con esta nueva ley, es posible diseñar vesículas con elasticidad predecible, optimizando la entrega en sinapsis o en zonas de inflamación sin depender del ensayo y error tradicional.
2. Diseño de células artificiales
Uno de los grandes desafíos en biología sintética es replicar el comportamiento de membranas naturales en sistemas artificiales. Comprender que el empaquetamiento lipídico es el parámetro clave permite construir membranas sintéticas que imiten fielmente la adaptabilidad celular, abriendo la puerta a células artificiales con funcionalidad real para diagnóstico o terapia.
3. Nanotecnología y nanoestructuras lipídicas
En nanotecnología, construir poros o canales lipídicos que regulen el paso selectivo de compuestos es una aplicación de alto valor. El colesterol ya fue identificado como un modulador clave en la constricción de poros a nivel nanométrico. Ahora, con un modelo predictivo del empaquetamiento, es posible diseñar nanoestructuras con propiedades mecánicas definidas de antemano.
4. Migración celular e inmunología
Investigaciones complementarias del CSIC han demostrado que alterar los niveles de colesterol en la membrana afecta la capacidad de migración de células inmunitarias como los linfocitos T, a través de receptores como CXCR4. Entender el empaquetamiento lipídico permite modelar y potencialmente modular esa migración, con aplicaciones directas en inmunoterapia y tratamiento de enfermedades inflamatorias.
El impacto para el ecosistema biotech en LATAM
Para founders que están construyendo en el espacio de biotech, healthtech o deeptech en América Latina, este tipo de hallazgos científicos representa oportunidades concretas. La región cuenta con laboratorios universitarios de excelencia y un talento científico creciente que muchas veces busca puentes hacia la aplicación comercial.
Comprender los mecanismos biofísicos fundamentales no es solo tarea de académicos: es la base sobre la que se construyen productos de alto impacto. Startups que integren este conocimiento en sus pipelines de I+D —ya sea en nanopartículas terapéuticas, biorreactores, diagnóstico molecular o biología sintética— estarán mejor posicionadas para competir globalmente.
Además, la validación experimental de este tipo de leyes universales facilita el trabajo con simulaciones computacionales, reduciendo la dependencia de costosos experimentos físicos en etapas tempranas. Eso es especialmente valioso en contextos donde el acceso a infraestructura de laboratorio es limitado.
Limitaciones y próximos pasos
Como en toda investigación de frontera, es importante ser preciso sobre el alcance actual. Las aplicaciones prácticas detalladas arriba son proyecciones basadas en el principio descubierto, pero requieren validación experimental adicional antes de ser trasladadas directamente a productos o terapias. El modelo biofísico es robusto, pero la biología celular real introduce capas de complejidad adicionales —proteínas de membrana, gradientes iónicos, interacciones con el citoesqueleto— que aún deben integrarse en el marco predictivo.
Dicho esto, contar con una ley física de base es un punto de partida muy diferente —y mucho más sólido— al empirismo ciego que caracterizó esta área durante décadas.
Conclusión
El descubrimiento de que la elasticidad de la membrana celular depende del empaquetamiento lipídico y no del tipo de lípido resuelve una de las paradojas más persistentes de la biofísica moderna. Con el colesterol identificado como modulador de ese empaquetamiento, los equipos de I+D en biomedicina, nanotecnología y biotecnología ahora cuentan con un modelo predictivo real sobre el que construir.
Para founders en deeptech y biotech, este avance no es solo una nota al pie en una revista científica: es una palanca de diseño que puede acortar ciclos de desarrollo, reducir costos experimentales y abrir nuevas ventanas de producto en mercados de alto impacto global. La ciencia de base sólida siempre termina siendo la mejor ventaja competitiva.
Profundiza estos temas con nuestra comunidad de founders en biotech, deeptech e IA aplicada.
Fuentes
- https://wwwhatsnew.com/2026/03/11/la-membrana-celular-deja-de-ser-caprichosa-el-colesterol-cambia-la-forma-pero-manda-el-empaquetamiento/ (fuente original)
- https://muyinteresante.okdiario.com/ciencia/el-colesterol-actua-como-modulador-clave-en-una-ley-fisica-universal-que-determina-cuando-una-membrana-celular-se-ablanda-o-se-endurece-como-si-fuera-una-puerta-que-regula-que-compuestos-pueden-pasar.html (fuente adicional)
- https://larepublica.es/2025/08/02/descubren-como-la-densidad-de-lipidos-determina-la-flexibilidad-de-las-membranas-celulares/ (fuente adicional)
- https://www.infobae.com/america/agencias/2025/12/12/el-colesterol-en-la-membrana-celular-afecta-a-la-capacidad-de-migrar-de-celulas-inmunitarias-donde-son-necesarias/ (fuente adicional)
- https://espanol.nichd.nih.gov/noticias/prensa/062023-avances-cientificos-DIR/slide4 (fuente adicional)
- http://www.csic.es/es/actualidad-del-csic/un-estudio-identifica-el-papel-clave-del-colesterol-en-la-migracion-de-las-celulas-del-sistema-inmunologico (fuente adicional)